Traduzione etichettatura dispositivi medici per packaging e artwork
- Nei dispositivi medici, i contenuti presenti su etichette, packaging e artwork rappresentano il primo livello di comunicazione regolatoria del prodotto. Da questi elementi dipendono l’identificazione del dispositivo, la corretta presentazione delle informazioni obbligatorie e la coerenza con quanto dichiarato nella documentazione approvata.
- La traduzione multilingua di questi materiali richiede un governo rigoroso dei contenuti. In questo contesto, la stabilità delle formulazioni, il controllo delle versioni e l’allineamento tra le lingue assumono un ruolo centrale. In parallelo, la verifica dei testi pre-stampa consente di ridurre il rischio di non conformità nella fase di distribuzione.
Etichettatura e packaging come requisito di conformità
I contenuti presenti su etichette, packaging e artwork dei dispositivi medici costituiscono il primo livello di evidenza regolatoria del prodotto. Da essi dipendono l’identificazione del dispositivo e la coerenza con la documentazione approvata ai fini MDR.
In presenza di più lingue, mercati o versioni, così come in caso di aggiornamenti regolatori, l’etichettatura non può essere gestita in modo frammentato. Un presidio linguistico strutturato assicura stabilità delle formulazioni, allineamento tra versioni e controllo pre-stampa, riducendo il rischio di discrepanze lungo la filiera distributiva.
Informazioni di etichetta e confezione primaria come elementi di verifica regolatoria
Nell’ambito dei dispositivi medici, etichettatura, packaging e artwork rappresentano superfici regolatorie verificabili. Si tratta di contenuti soggetti a controllo formale ai fini della conformità MDR. I testi che vi compaiono devono essere coerenti, linguisticamente stabili e riconducibili ai riferimenti presenti nella documentazione tecnica approvata. La traduzione interviene su questi elementi come operazione di controllo formale: rende confrontabili le versioni linguistiche, consente la tracciabilità delle formulazioni e supporta le attività di verifica in sede di audit, ispezione o rilascio multi-mercato.
- Coerenza tra etichettatura, simboli, avvertenze e istruzioni per l’uso.
- Stabilità delle formulazioni linguistiche su contenuti soggetti a verifica regolatoria
- Presidio delle versioni linguistiche in contesti multi-mercato
- Tracciabilità delle modifiche applicate ai contenuti di etichettatura
- Verifica linguistica dei testi destinati alla stampa e alla distribuzione
- Riduzione del rischio di rilievi ispettivi legati alla non conformità formale
Controllo linguistico e presidio regolatorio dell’etichettatura medicale
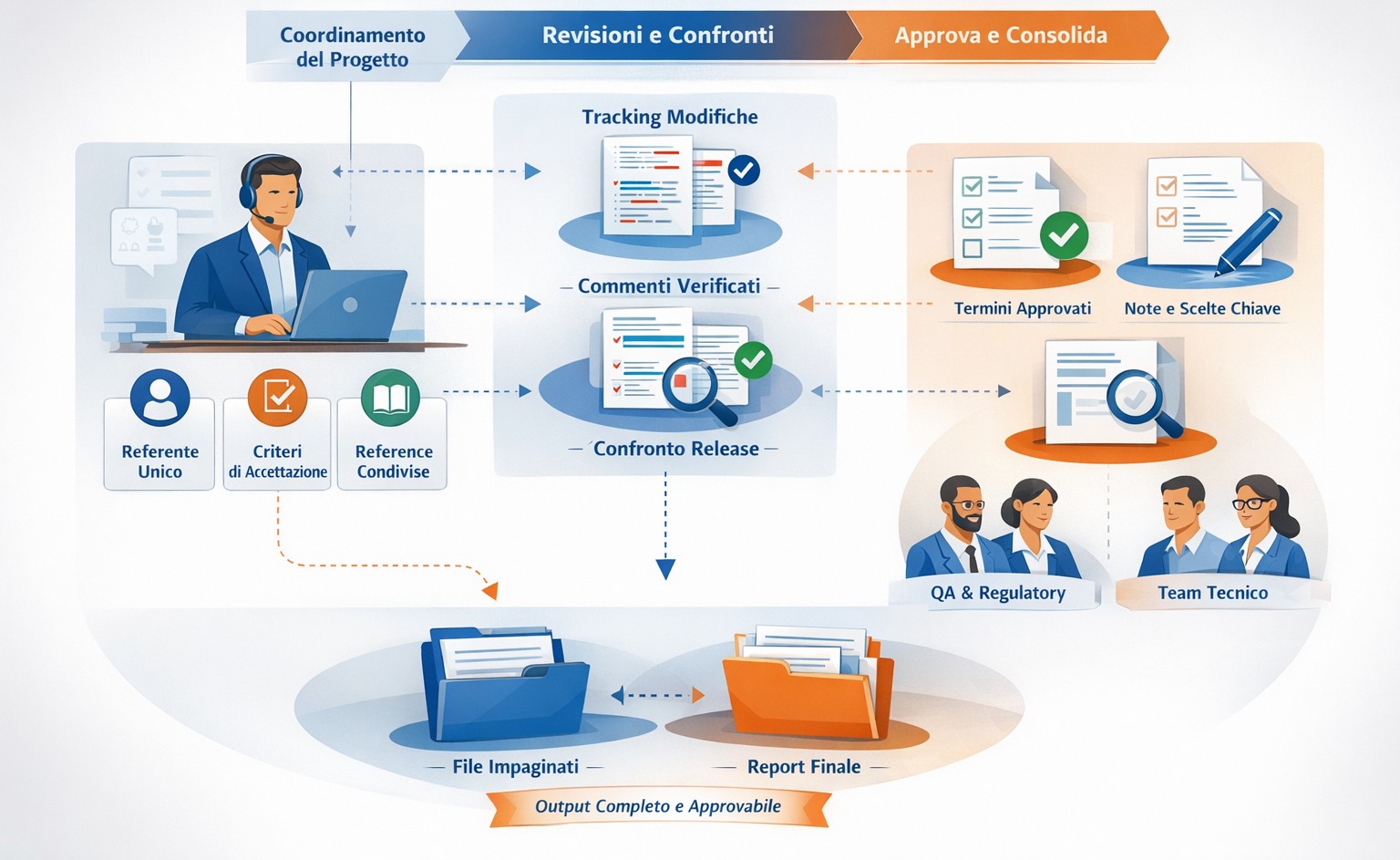
Ambito regolatorio MDR
Traduzione di contenuti regolatori in ambito medicale
Interventi su etichettatura, packaging e contenuti regolatori associati a dispositivi medici, svolti in contesti multi-mercato soggetti a requisiti MDR. Attività che hanno richiesto controllo linguistico formale, stabilità delle formulazioni e coerenza documentale tra versioni, in ambiti tecnologici e sanitari ad alta complessità.






