Traduzioni per il settore medicale e farmaceutico
I testi medicali hanno un impatto operativo: istruzioni, avvertenze e indicazioni devono restare inequivocabili, anche quando lo spazio è minimo, come in etichetta. Una formulazione ambigua può modificare l’interpretazione, innescare escalation interne e tradursi in ritardi, rilavorazioni o rischio regolatorio.
Documentazione clinica e documenti sanitari per ricerca e operation
Dispositivi medici: documentazione tecnica, istruzioni e IFU
Etichette e formazione medicale ad alta densità informativa regolatoria

Dove nascono gli errori nel medicale e come li preveniamo
Nel medicale gli inciampi raramente sono “errori evidenti”: nascono da micro-incoerenze tra documenti che devono combaciare. Un termine reso in modo diverso tra IFU ed etichetta, un’unità scritta con una convenzione non coerente, un’avvertenza che perde forza, un rimando interno che non torna. Quando poi entrano in gioco aggiornamenti e release successive, il rischio aumenta: basta una variazione non governata perché le correzioni si propaghino tra file correlati e i tempi si trasformino in rilavorazioni.
Per questo impostiamo un presidio specifico sul settore: reference condivise (glossari, acronimi, nomenclature) e controlli mirati su terminologia sensibile, numeri e unità, tabelle, simboli, avvertenze e riferimenti incrociati. Se il progetto include formati strutturati o impaginati (Word/Excel, PDF, InDesign), gestiamo il file handling in modo conservativo e chiudiamo con una verifica post-reintegro, così la coerenza resta stabile tra documentazione clinica, tecnica, etichette, istruzioni e materiali di formazione.
Deliverable chiave per traduzioni medicali e farmaceutiche
In questo settore non conta “che documento è”, ma come si collega agli altri: etichetta, istruzioni, tecnico e clinico devono combaciare su termini, unità, avvertenze e rimandi, spesso attraverso più release. Le card qui sotto sono i deliverable che incontriamo più spesso nei progetti medicali e farmaceutici; ogni voce rimanda alla pagina dedicata, con dettaglio su contenuti, formati e criticità operative.
- Istruzioni / IFU dispositivi medici — Istruzioni per l’uso orientate alla sicurezza: sequenze operative chiare, terminologia stabile, rimandi corretti.
- Etichette dispositivi medici — Testi ad alta densità informativa: unità, codici, avvertenze e coerenza tra elementi correlati.
- Documentazione tecnica dispositivi medici — Manuali e documentazione tecnica con vincoli di struttura, tabelle e coerenza interna.
- Documentazione clinica — Documenti per studi e attività cliniche: protocolli, modulistica e materiali a supporto della ricerca.
- Documenti sanitari — Documentazione operativa per strutture sanitarie, procedure e flussi assistenziali.
- Formazione medicale — Manuali, materiali di formazione e contenuti per personale medico e paramedico con terminologia coerente e istruzioni operative chiare.
Come gestiamo versioni, revisioni e approvazioni
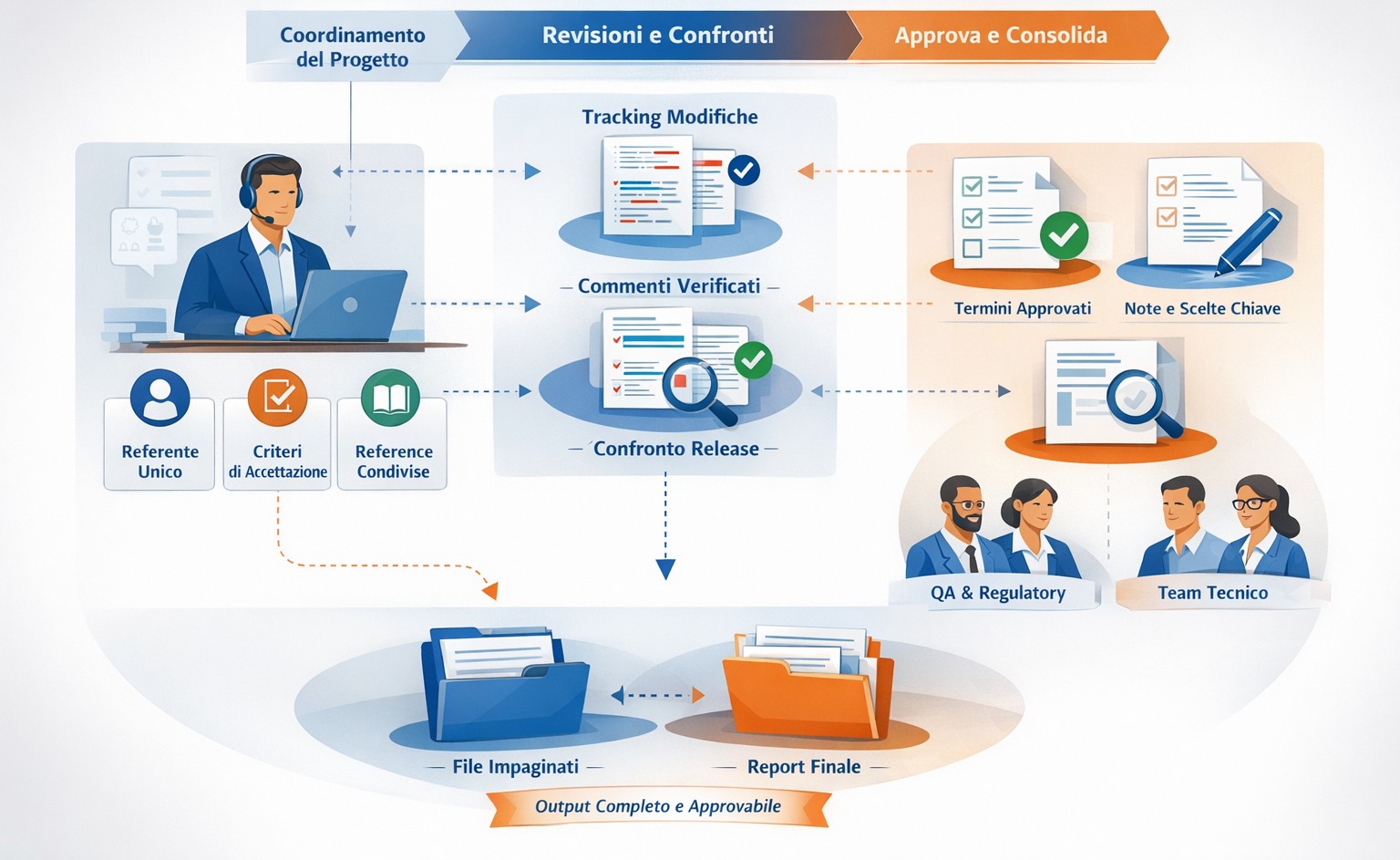
Regia unica, revisioni ordinate, output approvabili
Nei progetti medicali la traduzione è solo una parte del lavoro: ciò che pesa davvero è governare revisioni, stakeholder e versioni senza perdere controllo. Per questo impostiamo una regia unica sul progetto (un referente), definiamo reference e criteri di accettazione, e organizziamo i cicli di review in modo che chi approva trovi subito le informazioni utili, senza ricerche e senza ambiguità operative.
In pratica lavoriamo con pacchetti di revisione pronti per QA/Regulatory e team tecnici: file editabili con tracciamento modifiche, commenti gestiti e chiusi in modo ordinato, confronto tra release con evidenza di cosa è cambiato e dove, e consolidamento delle decisioni (termini approvati, scelte ricorrenti, note su punti critici) per le versioni successive. Quando c’è impaginazione o file strutturati, includiamo una verifica finale sul documento reintegrato, così l’output resta approvabile anche a valle del layout.
Oltre dispositivi e clinico: contenuti ad alta specializzazione
Nei progetti medicali e farmaceutici la documentazione principale (etichette, IFU, clinico, tecnico, formazione) convive spesso con contenuti ad alta specializzazione: pubblicazioni scientifiche, proprietà intellettuale, documenti etico-normativi e materiali farmacologici. In questi casi la qualità non si misura solo sulla lingua: conta la solidità del deliverable nel suo insieme, cioè coerenza tra definizioni, dati e responsabilità del testo.
Quando il perimetro si estende oltre dispositivi e clinico, ricorrono spesso questi ambiti. Cambia il pubblico e cambia la funzione del testo, ma la priorità resta la stessa: preservare significato, coerenza interna e tracciabilità, anche attraverso versioni successive.
Articoli scientifici e pubblicazioni
Lavoriamo su testi destinati a lettura e valutazione internazionale (abstract, paper, poster e materiali di submission). Il focus è precisione concettuale, terminologia disciplinare e coerenza tra testo e dati (figure, tabelle, appendici), evitando formulazioni che spostino il significato o alterino l’impianto metodologico.
Brevetti medico-scientifici e proprietà intellettuale
Nei brevetti la lingua è parte della struttura: definizioni, termini chiave e formulazioni devono rimanere stabili tra descrizione e rivendicazioni. Operiamo su ambiti come chimica, biologia, farmacologia e biogenetica, con attenzione a coerenza terminologica, uso rigoroso delle definizioni e controllo delle ricorrenze, perché anche una variazione minima può spostare il perimetro del testo.
Comitati Etici: scienza e cornice normativa
Verbali e documenti collegati ai Comitati Etici richiedono precisione e tracciabilità: decisioni, condizioni, richieste di integrazione e razionali devono restare leggibili e coerenti. Il presidio riguarda terminologia medico-normativa e tenuta dei passaggi che incidono su approvazioni, responsabilità e motivazioni.
Documentazione farmacologica e materiali tecnico-scientifici
Gestiamo schede, monografie, analisi chimiche e microbiologiche e documenti legati a protocolli sperimentali. Qui la qualità si misura su stabilità dei dati (unità, dosaggi, range), coerenza interna e continuità tra sezioni correlate, soprattutto quando il contenuto evolve per aggiornamenti e release successive.
HR e formazione in ambito sanitario
Traduciamo curricula, lettere specialistiche e materiali formativi per personale medico e paramedico. L’obiettivo è rendere il contenuto utilizzabile in contesti internazionali: struttura chiara, lessico corretto, tono professionale e coerenza con procedure e documentazione operativa di riferimento.
Importazione parallela: fogli illustrativi e documentazione AIFA (quando applicabile)
Nei progetti di importazione parallela la pratica AIFA può includere versioni tradotte del foglietto illustrativo e dell’etichettatura, oltre a allegati correlati, con vincoli stretti su tempi e corrispondenza tra documenti. Quando serve un’attestazione formale, possiamo emettere un certificato di veridicità a valle di un doppio passaggio (traduzione + correzione bozze da secondo linguista qualificato), così la versione finale resta allineata all’originale e coerente in ogni punto.
Se stai gestendo un iter con vincoli formali, possiamo fare una valutazione iniziale su documenti, formati, versioni e punti critici prima di avviare la lavorazione.
Esempi di progetti e deliverable
Una selezione di progetti medicali in contesti regolati: dispositivi certificati, imaging diagnostico, contenuti clinici e farmaceutici multilingua. In comune hanno la stessa esigenza: versioni approvabili, coerenza tra documenti collegati e controllo dei dettagli che incidono su sicurezza, uso e compliance.