Traduzione della documentazione clinica e di sicurezza
- La documentazione clinica e di sicurezza comprende testi utilizzati direttamente nei processi di sperimentazione, monitoraggio e sorveglianza. Consensi informati, protocolli, CRF e report di sicurezza sono strumenti operativi, destinati a personale clinico, a chi cura la formazione del personale sanitario, enti di controllo e sistemi di farmacovigilanza.
- La traduzione agisce su materiali che producono effetti interpretativi: orientano decisioni cliniche, valutazioni di rischio e continuità informativa nel tempo. Per questo deve garantire precisione semantica, leggibilità controllata e stabilità delle formulazioni lungo l’intero ciclo clinico e di sorveglianza.

Traduzione clinica e di sicurezza: quando il linguaggio supporta le decisioni vitali
Nella documentazione clinica e di sicurezza, il linguaggio non accompagna il processo: lo condiziona. Consensi informati, protocolli di studio, segnalazioni di eventi avversi e report di sicurezza non sono testi consultivi, ma strumenti attraverso cui vengono assunte decisioni cliniche, valutati rischi e formalizzate responsabilità. La traduzione interviene su contenuti letti, interpretati e utilizzati da soggetti diversi, in momenti diversi, spesso a distanza di tempo dall’evento originario.
In questo scenario, la traduzione non è un passaggio accessorio. Incide direttamente sulla possibilità di verificare rimandi, corrispondenze e dipendenze interne, soprattutto quando il fascicolo viene riesaminato, aggiornato o sottoposto a controllo nel tempo.
Dove nascono le criticità nella documentazione clinica e di sicurezza
Negli studi clinici e nelle attività di farmacovigilanza, la documentazione non è neutra. Errori di allineamento, formulazioni instabili o incoerenze tra testi possono compromettere la lettura dei dati, rallentare i processi decisionali o generare criticità nelle fasi di revisione e controllo. Il rischio non è immediato, ma emerge nel tempo, quando i documenti vengono riutilizzati, aggiornati o confrontati tra loro.
Interveniamo su questi insiemi documentali per evitare che le dipendenze tra testi diventino punti di frizione. Lavoriamo su protocolli, CRF, consensi informati, segnalazioni di eventi avversi e report di sicurezza come parti di un unico sistema, assicurando continuità clinica, coerenza terminologica e leggibilità dei rimandi tra documenti utilizzati in contesti regolatori e decisionali diversi.
- Prevenzione di incongruenze tra documenti che regolano lo studio clinico e la safety
- Allineamento dei rimandi tra protocolli, CRF e materiali informativi
- Coerenza tra procedure cliniche, criteri di valutazione ed eventi avversi
- Gestione degli aggiornamenti senza perdita di continuità tra versioni
- Stabilità terminologica nelle diverse lingue di lavoro
- Lettura trasversale dell’insieme documentale a supporto di revisioni e controlli
Un flusso di lavoro pensato per documenti interdipendenti
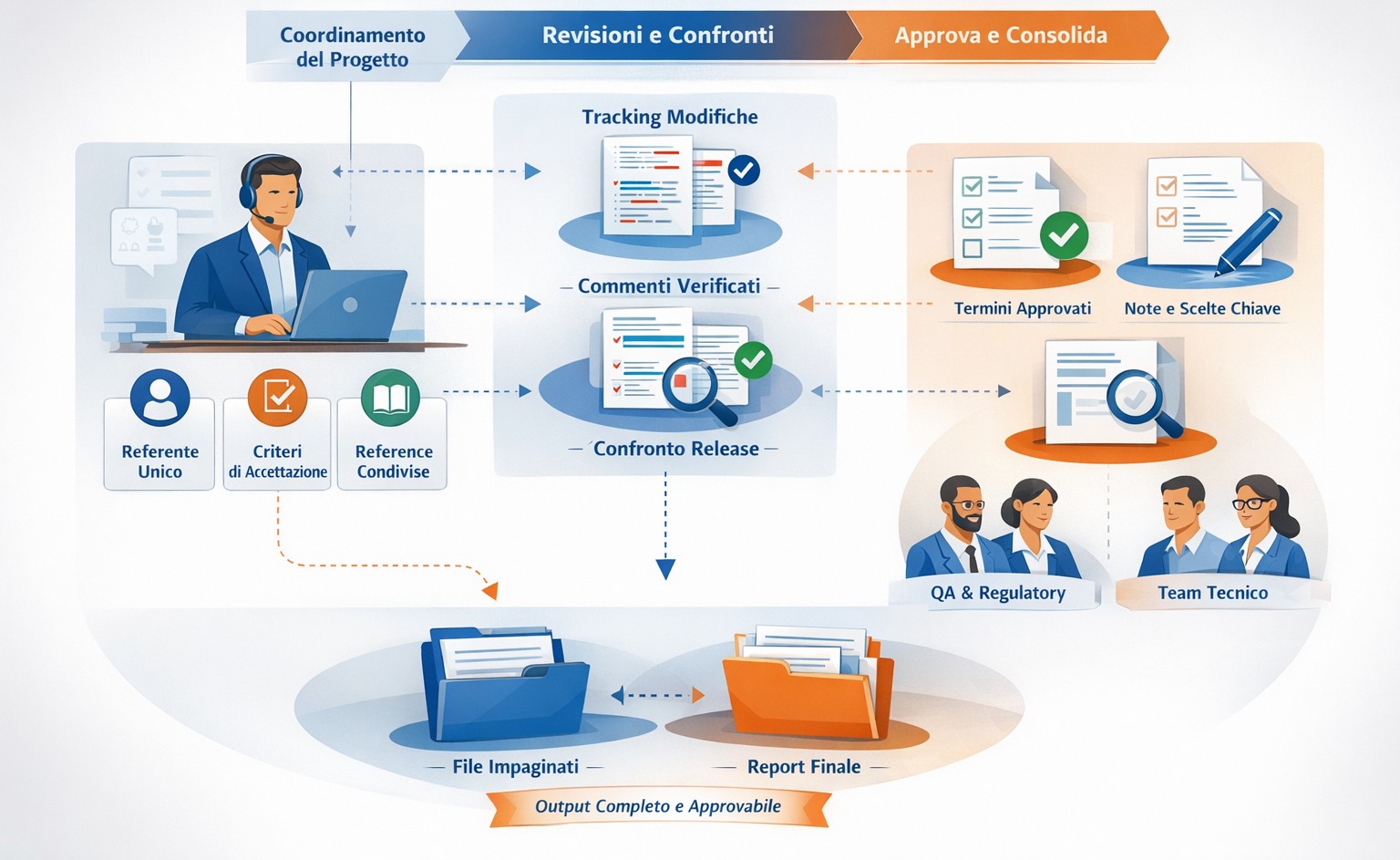
Contesto clinico regolato
Progetti sanitari multicanale e multilingua ad alta complessità
I casi presentati riguardano programmi di comunicazione in ambito sanitario e life sciences che integrano documentazione, contenuti audiovisivi, presentazioni istituzionali, asseverazioni e collaborazioni editoriali su ampia scala. Si tratta di progetti distribuiti su più media, sviluppati in decine di lingue e composti da volumi rilevanti di contenuti, spesso prodotti e aggiornati in parallelo. La complessità non è solo linguistica, ma organizzativa: coordinare flussi, formati, lingue e funzioni mantenendo coerenza, affidabilità e continuità nel tempo.






