Traductions pour le secteur médical et pharmaceutique
Les textes médicaux ont un impact opérationnel direct : instructions, avertissements et indications doivent rester parfaitement clairs, même lorsque l’espace est restreint, comme sur une étiquette. Une formulation ambiguë peut modifier l’interprétation, provoquer des escalades internes et entraîner des retards, des reprises ou un risque réglementaire.
Documentation clinique et documents de santé destinés à la recherche et aux activités opérationnelles
Dispositifs médicaux : documentation technique, instructions et notices IFU
Étiquetage et formation médicale à forte densité d’informations réglementaires

Où naissent les erreurs en milieu médical et comment nous les évitons
Dans le secteur médical, les erreurs sont rarement « visibles » : elles résultent le plus souvent de micro-incohérences entre des documents qui doivent rester parfaitement cohérents. Un terme formulé différemment entre IFU et étiquetage, une unité exprimée selon une convention non alignée, un avertissement affaibli, un renvoi interne défaillant. Lorsque s’ajoutent des mises à jour et des versions successives, le risque s’amplifie : une variation non maîtrisée suffit à propager des écarts entre des fichiers liés et à transformer les délais en reprises.
C’est pourquoi nous mettons en place un dispositif dédié au secteur : référentiels partagés (glossaires, acronymes, nomenclatures) et contrôles ciblés sur la terminologie sensible, les chiffres et unités, les tableaux, les symboles, les avertissements et les renvois croisés. Lorsque le projet inclut des formats structurés ou mis en page (Word/Excel, PDF, InDesign), nous gérons les fichiers de manière conservatrice et clôturons par une vérification post-réintégration, afin de maintenir une cohérence durable entre documentation clinique, technique, étiquetage, instructions et supports de formation.
Livrables clés des traductions médicales et pharmaceutiques
Dans ce secteur, ce qui compte n’est pas « le type de document », mais la façon dont il s’articule avec les autres : étiquetage, instructions, documentation technique et clinique doivent rester parfaitement cohérents en termes de terminologie, d’unités, d’avertissements et de renvois, souvent sur plusieurs versions successives. Les cartes ci-dessous présentent les livrables les plus courants dans les projets médicaux et pharmaceutiques ; chaque élément renvoie à une page dédiée, avec le détail des contenus, des formats et des points de vigilance opérationnels.
- Instructions / IFU pour dispositifs médicaux — Instructions d’utilisation axées sur la sécurité : séquences opérationnelles claires, terminologie stable et renvois fiables.
- Étiquetage des dispositifs médicaux — Textes à forte densité d’information : unités, codes, avertissements et cohérence entre éléments liés.
- Documentation technique des dispositifs médicaux — Manuels et documentation technique soumis à des contraintes de structure, de tableaux et de cohérence interne.
- Documentation clinique — Documents destinés aux études et aux activités cliniques : protocoles, formulaires et supports de recherche.
- Documents de santé — Documentation opérationnelle destinée aux établissements de santé, aux procédures et aux parcours de soins.
- Formation médicale — Manuels, supports de formation et contenus destinés au personnel médical et paramédical, avec une terminologie cohérente et des instructions opérationnelles claires.
Comment nous gérons les versions, les révisions et les validations
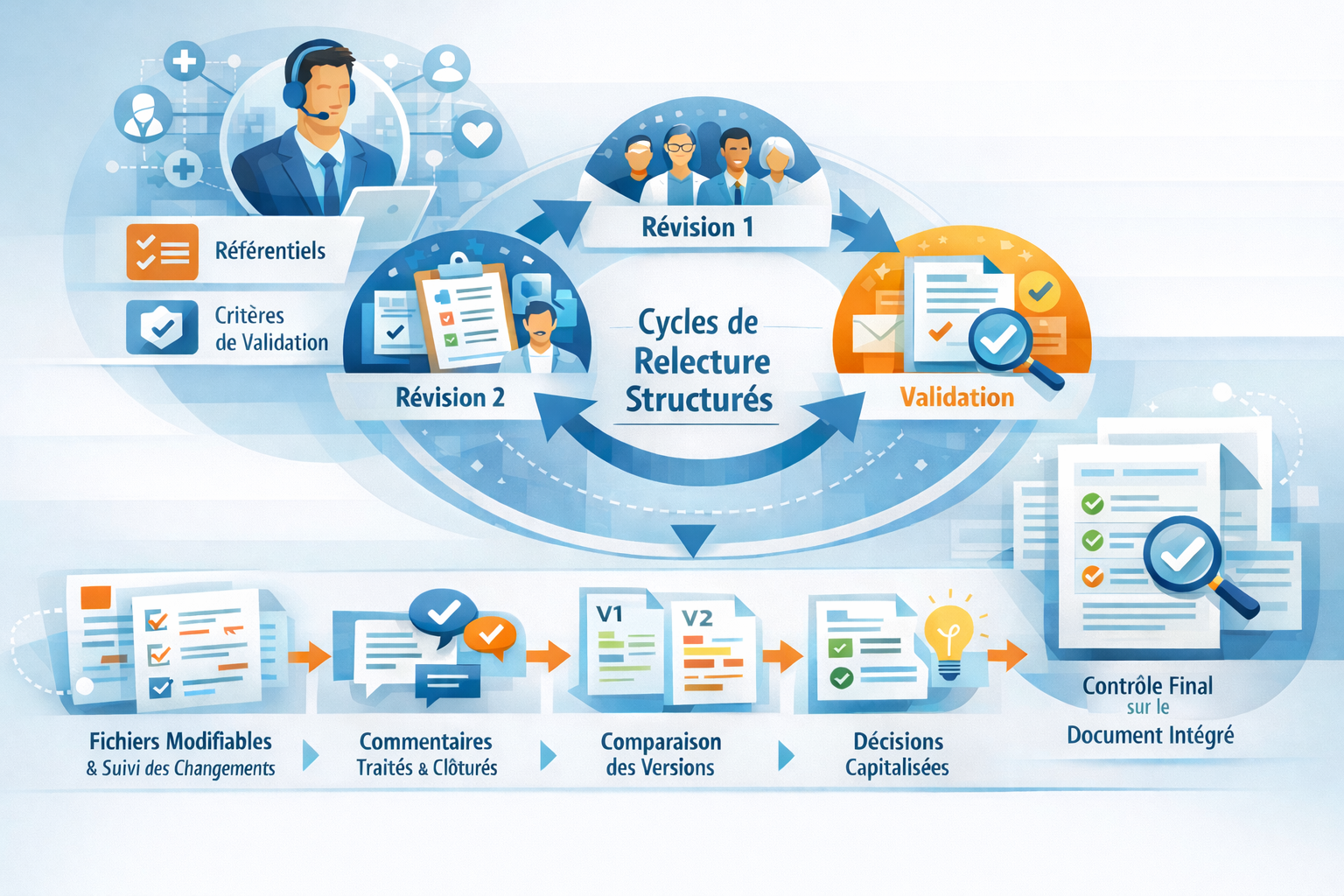
Pilotage centralisé, révisions structurées, livrables prêts à validation
Dans les projets médicaux, la traduction ne représente qu’une partie du travail : l’enjeu principal consiste à piloter révisions, parties prenantes et versions sans perte de contrôle. C’est pourquoi nous mettons en place un pilotage centralisé du projet (un interlocuteur unique), définissons des référentiels et des critères d’acceptation, et structurons les cycles de revue afin que les validateurs identifient immédiatement les informations utiles, sans recherches inutiles ni ambiguïtés opérationnelles.
Concrètement, nous travaillons avec des lots de révision prêts pour les équipes QA/Regulatory et techniques : fichiers éditables avec suivi des modifications, commentaires traités et clôturés de manière ordonnée, comparaison entre versions mettant clairement en évidence ce qui a évolué et où, et consolidation des décisions (terminologie validée, choix récurrents, notes sur les points sensibles) pour les versions suivantes. Lorsque le projet inclut de la mise en page ou des formats structurés, nous intégrons une vérification finale sur le document réintégré, afin de garantir un livrable pleinement validable après le layout.
Au-delà des dispositifs médicaux et du champ clinique : contenus hautement spécialisés
Dans les projets médicaux et pharmaceutiques, la documentation principale (étiquetage, IFU, contenus cliniques et techniques, formation) cohabite souvent avec des contenus hautement spécialisés : publications scientifiques, propriété intellectuelle, documents éthico-réglementaires et contenus pharmaceutiques. Dans ces contextes, la qualité ne se limite pas à la langue : elle repose sur la solidité globale du livrable, c’est-à-dire sur la cohérence entre les définitions, les données et les responsabilités portées par le texte.
Lorsque le périmètre s’étend au-delà des dispositifs médicaux et du champ clinique, ces domaines reviennent fréquemment. Le public change, la fonction du texte évolue, mais la priorité demeure : préserver le sens, la cohérence interne et la traçabilité, y compris au fil des versions successives.
Articles scientifiques et publications
Nous travaillons sur des textes destinés à une lecture et à une évaluation à l’échelle internationale (abstracts, articles, posters et dossiers de soumission). La priorité est donnée à la précision conceptuelle, à la terminologie disciplinaire et à la cohérence entre le texte et les données (figures, tableaux, annexes), en évitant toute formulation susceptible de déplacer le sens ou de modifier l’approche méthodologique.
Brevets médico-scientifiques et propriété intellectuelle
Dans les brevets, la langue constitue un élément structurel : définitions, termes clés et formulations doivent rester parfaitement stables entre la description et les revendications. Nous intervenons dans des domaines tels que la chimie, la biologie, la pharmacologie et la biogénétique, avec une attention constante portée à la cohérence terminologique, à l’usage rigoureux des définitions et au contrôle des occurrences, car la moindre variation peut modifier le périmètre du texte.
Comités d’éthique : science et cadre réglementaire
Les procès-verbaux et les documents associés aux comités d’éthique exigent rigueur et traçabilité : décisions, conditions, demandes de compléments et justifications doivent rester claires et cohérentes. Le dispositif porte sur la terminologie médico-réglementaire et sur la solidité des enchaînements ayant un impact sur les validations, les responsabilités et les motivations.
Documentation pharmacologique et documents technico-scientifiques
Nous prenons en charge des fiches, des monographies, des analyses chimiques et microbiologiques, ainsi que des documents liés aux protocoles expérimentaux. La qualité s’apprécie ici à la stabilité des données (unités, dosages, plages de valeurs), à la cohérence interne et à la continuité entre les sections connexes, en particulier lorsque les contenus évoluent au fil des mises à jour et des versions successives.
RH et formation dans le secteur de la santé
Nous traduisons des CV, des lettres spécialisées et des supports de formation destinés au personnel médical et paramédical. L’objectif est de rendre les contenus utilisables dans des contextes internationaux : structure claire, terminologie adéquate, ton professionnel et cohérence avec les procédures et la documentation opérationnelle de référence.
Importation parallèle : notices et documentation de l’AIFA (le cas échéant)
Dans les projets d’importation parallèle, le dossier AIFA peut inclure des versions traduites de la notice et de l’étiquetage, ainsi que des annexes associées, avec des contraintes strictes en termes de délais et de correspondance entre les documents. Lorsqu’une attestation formelle est requise, nous pouvons délivrer un certificat de fidélité à l’issue d’un double processus de contrôle (traduction suivie d’une relecture par un second linguiste qualifié), afin que la version finale reste strictement alignée sur l’original et cohérente dans toutes ses parties.
Si vous gérez une procédure soumise à des contraintes formelles, nous pouvons réaliser une évaluation initiale des documents, des formats, des versions et des points sensibles avant d’engager les travaux.
Exemples de projets et de livrables
Une sélection de projets médicaux réalisés dans des contextes réglementés : dispositifs certifiés, imagerie diagnostique, contenus cliniques et pharmaceutiques multilingues. Ils partagent tous la même exigence : des versions prêtes à validation, une cohérence entre les documents liés et une maîtrise rigoureuse des détails ayant un impact sur la sécurité, l’usage et la conformité.