Traduction de l’étiquetage des dispositifs médicaux pour le packaging et les artworks
- Dans le domaine des dispositifs médicaux, les contenus figurant sur les étiquettes, le packaging et les artworks constituent le premier niveau de communication réglementaire du produit. De ces éléments dépendent l’identification du dispositif, la présentation correcte des informations obligatoires et la cohérence avec les contenus déclarés dans la documentation approuvée.
- La traduction multilingue de ces supports suppose une gouvernance rigoureuse des contenus. Dans ce contexte, la stabilité des formulations, le contrôle des versions et l’alignement entre les langues jouent un rôle central. En parallèle, la vérification des textes en phase de prépresse permet de réduire le risque de non-conformité au moment de la mise sur le marché.
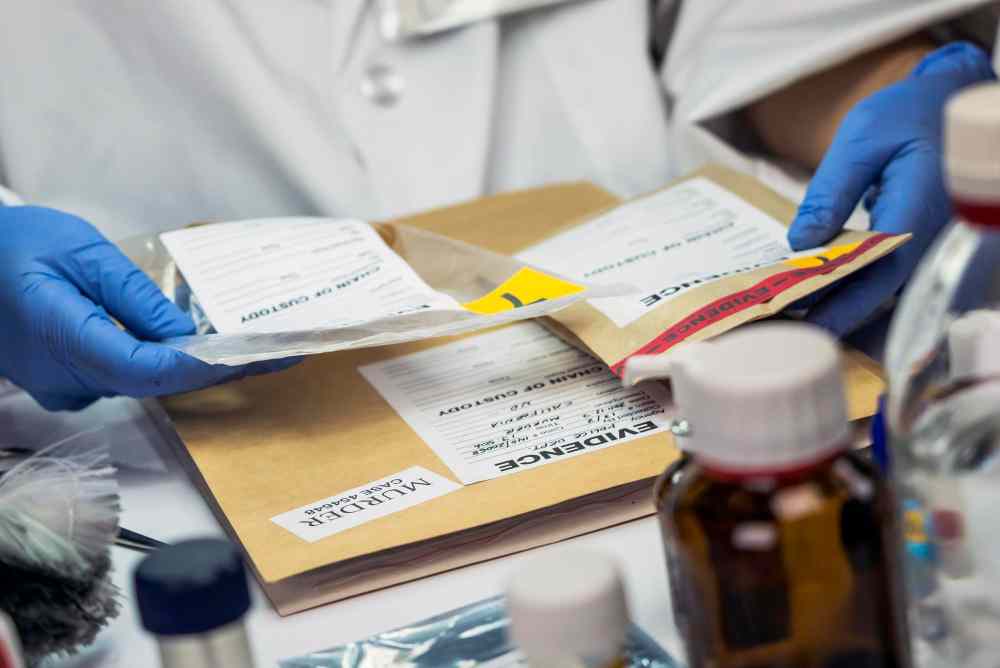
Étiquetage et packaging en tant qu’exigence de conformité
Les contenus figurant sur les étiquettes, le packaging et les artworks des dispositifs médicaux constituent le premier niveau de preuve réglementaire du produit. Ils conditionnent l’identification du dispositif ainsi que la cohérence avec la documentation approuvée au titre du MDR.
En présence de plusieurs langues, marchés ou versions, comme en cas de mises à jour réglementaires, l’étiquetage ne peut être géré de manière fragmentée. Une gouvernance linguistique structurée garantit la stabilité des formulations, l’alignement entre les versions et le contrôle en phase de prépresse, tout en réduisant le risque de divergences tout au long de la chaîne de distribution.
Les informations d’étiquetage et de conditionnement primaire comme éléments de vérification réglementaire
Dans le domaine des dispositifs médicaux, l’étiquetage, le packaging et les artworks constituent des supports réglementaires vérifiables.
Il s’agit de contenus soumis à un contrôle formel au titre de la conformité MDR.
Les textes qui y figurent doivent être cohérents, linguistiquement stables et directement rattachables aux références présentes dans la
documentation technique
approuvée.
La traduction intervient sur ces éléments en tant qu’opération de contrôle formel : elle permet de comparer les versions linguistiques, d’assurer la traçabilité des formulations et de soutenir les activités de vérification lors des audits, inspections ou déploiements multi-marchés.
- Cohérence entre l’étiquetage, les symboles, les avertissements et les instructions d’utilisation
- Stabilité des formulations linguistiques pour des contenus soumis à un contrôle réglementaire
- Gouvernance des versions linguistiques dans des environnements multi-marchés
- Traçabilité des modifications apportées aux contenus d’étiquetage
- Vérification linguistique des textes destinés à l’impression et à la diffusion
- Réduction du risque de constats d’inspection liés à une non-conformité formelle
Contrôle linguistique et gouvernance réglementaire de l’étiquetage médical
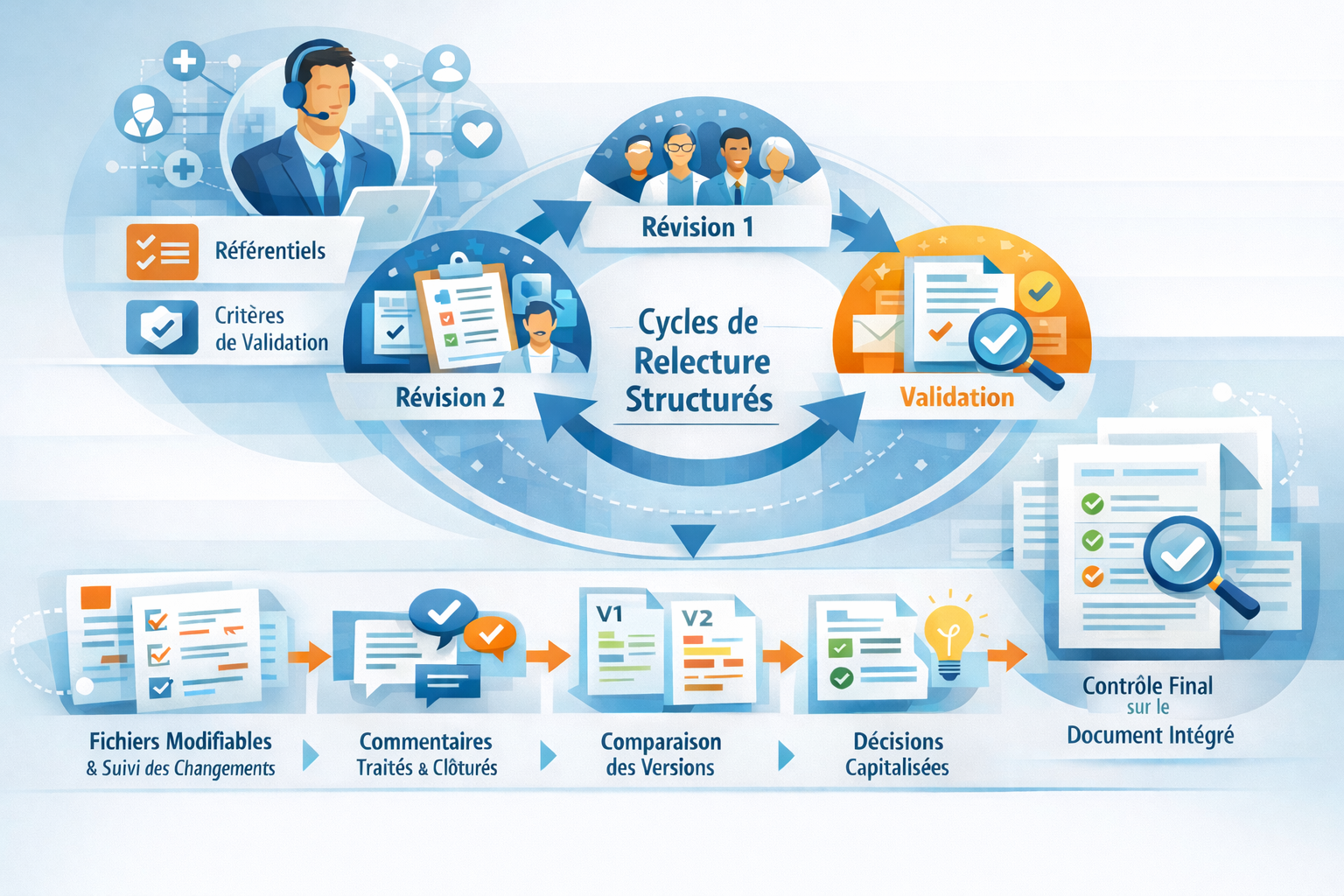
Cadre réglementaire MDR
Traduction de contenus réglementaires dans le domaine médical
Interventions portant sur l’étiquetage, le packaging et les contenus réglementaires associés aux dispositifs médicaux, menées dans des contextes multi-marchés soumis aux exigences du MDR. Des activités impliquant un contrôle linguistique formel, la stabilité des formulations et une cohérence documentaire entre les versions, dans des environnements technologiques et sanitaires à forte complexité.






