Traduction de la documentation clinique et de sécurité
- La documentation clinique et de sécurité rassemble des textes utilisés au cœur des activités d’essai, de suivi et de surveillance. Les consentements éclairés, protocoles, CRF et rapports de sécurité constituent des outils opérationnels destinés aux équipes cliniques, aux acteurs de la formation des professionnels de santé, aux autorités de contrôle et aux dispositifs de pharmacovigilance.
- La traduction intervient sur des contenus dont la portée interprétative est directe : ils influencent les décisions cliniques, l’analyse des risques et la continuité de l’information dans le temps. Elle suppose donc une rigueur terminologique, une lisibilité maîtrisée et une cohérence rédactionnelle constante tout au long du cycle clinique et des phases de surveillance.

Traduction clinique et de sécurité : le langage au service de décisions vitales
En matière de documentation clinique et de sécurité, le langage joue un rôle déterminant. Consentements éclairés, protocoles d’étude, déclarations d’événements indésirables et rapports de sécurité ne relèvent pas de la simple information : ce sont des supports opérationnels à partir desquels s’élaborent des décisions cliniques, s’apprécient les risques et se formalisent les responsabilités. La traduction concerne des contenus consultés et exploités par des intervenants différents, à des étapes distinctes, parfois bien après les faits initiaux.
Dans ce cadre, la traduction ne saurait être considérée comme secondaire. Elle conditionne la possibilité de contrôler les renvois, les cohérences et les relations internes, en particulier lorsque le dossier est réexaminé, actualisé ou soumis à des procédures de contrôle dans la durée.
Où se situent les principales zones de vigilance en documentation clinique et de sécurité
Dans les essais cliniques et en pharmacovigilance, la documentation joue un rôle actif. Des écarts d’alignement, des formulations fluctuantes ou des divergences entre documents peuvent fausser l’exploitation des données, ralentir les arbitrages ou compliquer les phases de révision et de contrôle. Les effets ne sont pas toujours immédiats : ils apparaissent dans le temps, lorsque les documents sont repris, actualisés ou mis en regard les uns des autres.
Notre intervention vise à prévenir les dysfonctionnements liés aux interactions entre documents. Protocoles, CRF, consentements éclairés, déclarations d’événements indésirables et rapports de sécurité sont abordés comme les éléments d’un dispositif documentaire cohérent, afin de préserver la continuité clinique, l’homogénéité terminologique et la clarté des renvois entre des supports utilisés dans des cadres réglementaires et décisionnels distincts.
- Prévention des incohérences entre les documents encadrant l’étude clinique et la sécurité
- Cohérence des renvois entre protocoles, CRF et documents d’information
- Alignement des procédures cliniques, des critères d’évaluation et des événements indésirables
- Maîtrise des mises à jour sans discontinuité entre les versions
- Homogénéité terminologique dans les différentes langues de travail
- Analyse transversale de l’ensemble documentaire dans le cadre des revues et des contrôles
Un dispositif de travail adapté à des documents interdépendants
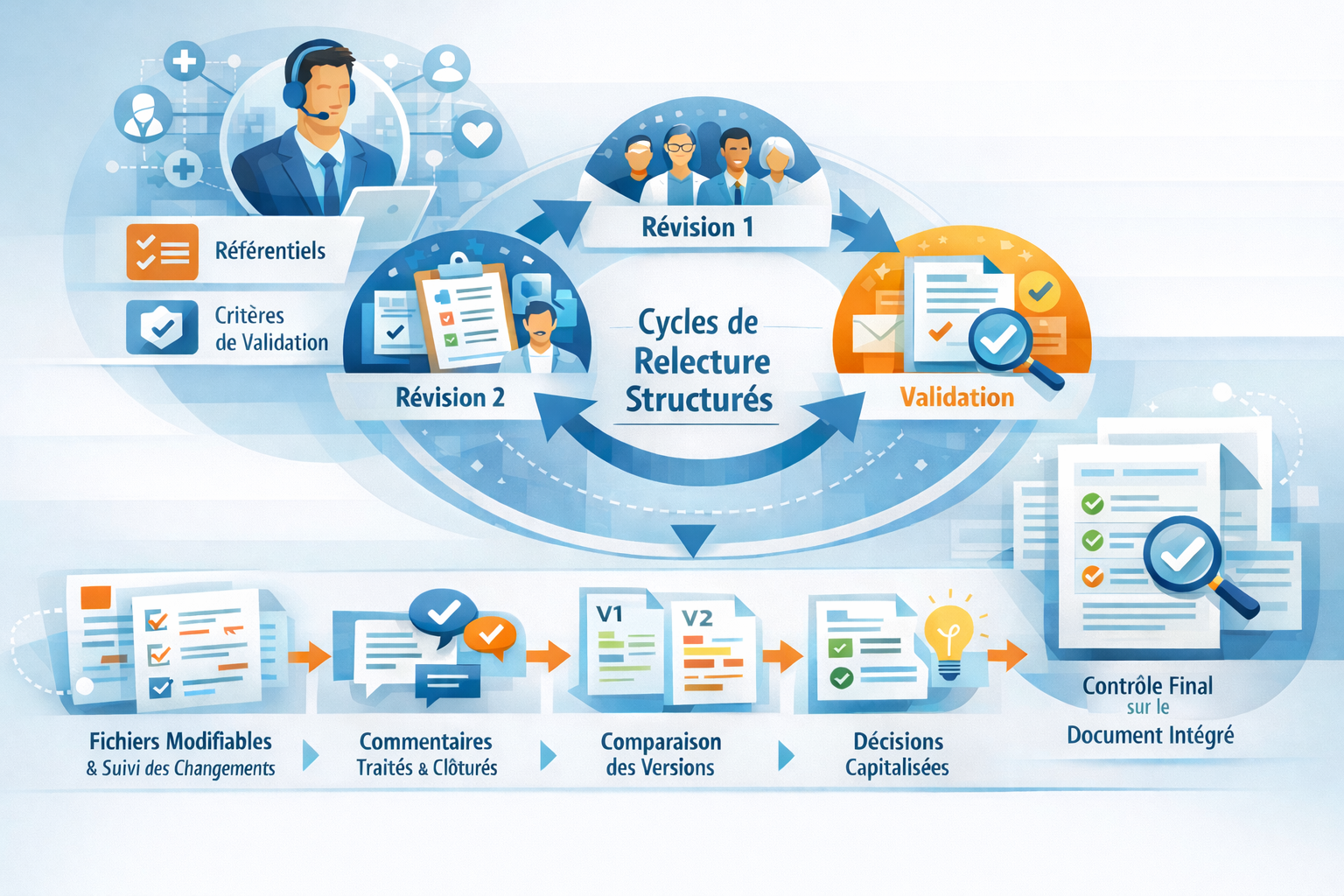
Environnement clinique réglementé
Projets de santé multicanal et multilingue à forte complexité
Les exemples présentés relèvent de programmes de communication en santé et en life sciences, combinant documentation, contenus audiovisuels, supports institutionnels, attestations et partenariats éditoriaux à grande échelle. Ces projets s’inscrivent dans des dispositifs multicanaux, déployés dans de nombreuses langues et fondés sur des volumes conséquents de contenus, fréquemment produits et mis à jour en parallèle. La complexité dépasse la seule dimension linguistique : elle tient à la coordination des flux, des formats, des langues et des fonctions, tout en assurant la cohérence, la fiabilité et la continuité dans la durée.






